成大利宝®乙脑灭活疫苗(Vero细胞)
所属分类:
已上市产品
- 产品描述
-
成大利宝®乙脑灭活疫苗
(Vero细胞)
成大利宝®乙脑灭活疫苗于2008年上市,接种本疫苗后可刺激机体产生抗乙型脑炎病毒的免疫力,用于预防流行性乙型脑炎。产品已出口至泰国。疫苗不含活病毒,适用人群更加广泛,具有较好免疫原性,更加纯净安全。
产品特性

一、适用人群更加广泛
成大利宝®乙脑灭活疫苗不含活病毒,无毒力恢复致病的风险,避免了疫苗相关病例及疫苗衍生病毒的风险。不仅适用于健康的适龄儿童,还可用于抗生素过敏、免疫缺陷、免疫功能低下或正在接受免疫抑制治疗的特殊人群,适用人群更加广泛。欧洲、北美洲、日本等国家和地区主要批准和使用乙脑灭活疫苗(Vero细胞)。
二、良好的免疫原性
成大利宝®乙脑灭活疫苗具有较好的免疫原性,其在中国Ⅲ期临床试验结果中的抗体阳转率平均高达90%以上,于泰国临床试验结果中的抗体阳转率为100%。
三、纯净安全
成大利宝®通过从配方中去除抗生素、明胶等成分,消除由该等成分导致过敏及其他不良副作用的潜在风险。生产工艺中使用β-丙内酯代替甲醛,这有助于疫苗实现更加彻底的病毒灭活,并能够水解为对人体无害的普通化合物。成大利宝®采用Vero细胞作为细胞基质,可通过生物反应器进行培养,无需宰杀动物。因此,培养细胞的质量较易控制且培养过程受污染的机会较低。
临床数据

一、大规模安全性观察
负责单位:国家CDC免疫规划中心
现场:江苏、浙江、云南、宁夏四省,每省1-2个区县
观察对象:8月龄-2岁健康儿童,3608人
结论:
1. 8月龄:接种成大利宝®后主要表现为轻、中度发热,局部反应主要为红肿无严重不良反应,第二剂次不良反应发生率少于第一剂;
2. 2岁:接种成大利宝®和减毒活疫苗后局部未见不良反应,全身不良反应仅见轻中度发热,两者差异无统计学意义。
—— 尹遵栋,等. 中国疫苗和免疫,2011,17(3): 195-200.
二、两种乙脑疫苗序贯免疫的安全性评价
负责单位:天津市CDC
观察对象:9月龄-2岁健康儿童,5019人
结论:减毒活疫苗和灭活疫苗序贯免疫有良好的安全性
—— 李永成,等. 中国疫苗和免疫,2011,17(2): 155-157.
成大利宝®III期临床血清学研究

成大利宝®免疫原性良好,明显高于国内同类产品
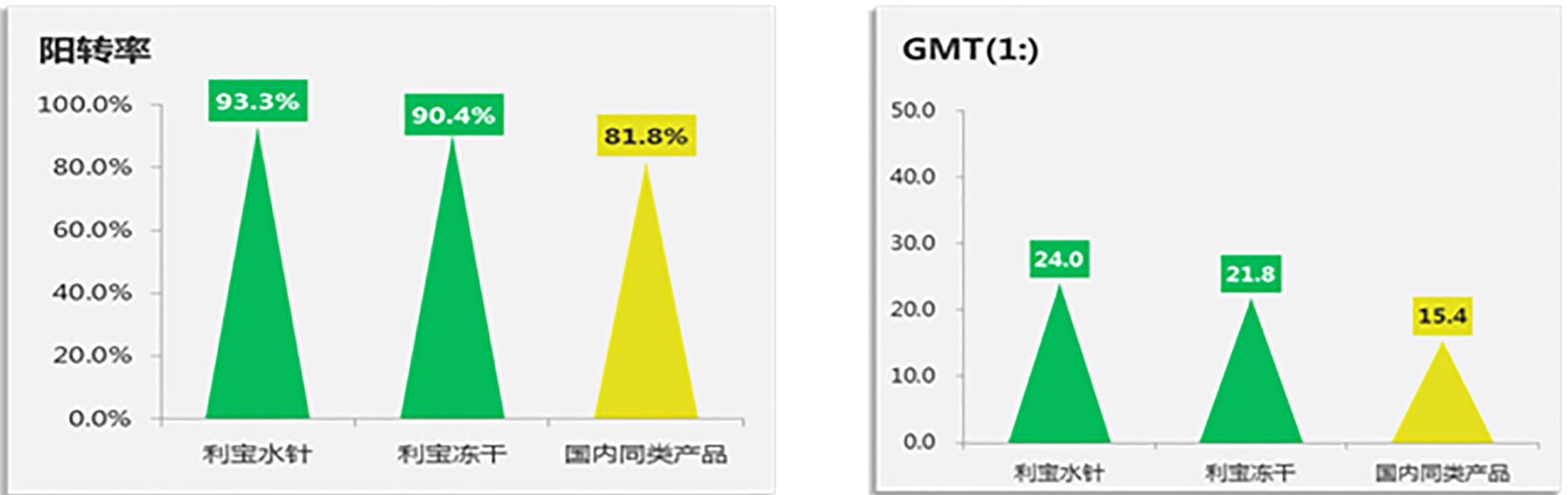
—— 周荔葆,等. 中国生物制品学杂志,2009,22(8): 809-811.
上一页
上一页
其他产品